肖景波,王朋濤,胡彩華,王衛東
( 南陽東方應用化工研究所,河南南陽 473000)
摘 要:在以氨或碳銨法工藝制備鎂鹽過程中有大量的銨氮廢水產生,對環境造成了污染。為了尋找銨氮廢水的合適的綜合利用途徑,以菱苦土為分解劑與廢水中的銨鹽反應,研究了菱苦土加入量、反應時間和溫度條件對廢水中銨鹽分解率的影響。結果表明,在優化工藝條件下銨鹽分解率達到 90% 以上。優化工藝條件的確定,為以氨法制備氫氧化鎂或以碳銨法制備堿式碳酸鎂生產過程中工藝廢水的處理奠定了理論基礎,也為氨的回收及循環利用提供了條件。
關鍵詞:菱苦土; 銨鹽; 分解率
Abstract:A great deal of wastewater containing ammonium and nitrogen will be produced in the production process of magnesium salts by ammonia or carbon-ammonia technologies,which can pollute the environment. Magnesia compounds that acted as decomposition regent reacted with ammonium salts existing in the wastewater to achieve a comprehensive utilization of wastewater. Influences of amounts of magnesia,reaction time,and temperature on the decomposition rate of ammonium salts were investigated. Results indicated that more than 90% of ammonium salts in the wastewater can be decomposed un-der the optimized conditions ,which established a theoretical foundation for wastewater treatment in the process of synthesi-zing magnesium hydroxide via an ammonic route or basic magnesium carbonate via a carbon-ammonia technology. Moreover,this method also provided conditions for ammonia recovery and recycle.
Key words:magnesia;ammonium salts;decomposition rate
在以氨法制備氫氧化鎂或以碳銨法制備堿式碳酸鎂生產過程中會產生大量工藝廢水,這種工藝廢水主要是母液和洗水,其中含有 ( NH4)2SO4或NH4Cl。對于含銨廢水現行的綜合利用方法主要有兩種: 一是通過蒸發濃縮、冷卻結晶收得硫酸銨或氯化銨[1],但處理過程耗能高,硫酸銨或氯化銨附加值低,從經濟角度考慮可行性不大; 二是用石灰乳與廢液中的硫酸銨或氯化銨反應,使銨鹽得以分解轉化為氨,再經吸收制得氨水[2]。石灰乳法處理成本低,銨分解率較高,但存在如下問題: 1) 以石灰乳分解硫酸銨時會產生大量的二水硫酸鈣,作為固體廢棄物排放會對環境造成影響; 2) 以石灰乳分解氯化銨時,銨分解后產生的殘液主要成分為氯化鈣,如予以回收同樣存在著處理過程耗能高、產品附加值低的問題,如予以排放同樣會對環境造成二次污染。為了尋找一條經濟、環保、可行的銨氮廢水綜合利用途徑,筆者以菱苦土( MgO) 為處理劑,進行了銨氮廢水中銨鹽分解條件的研究。
1 實驗部分
1.1 實驗方法
實驗原料: 菱苦土,含 MgO 質量分數為85%,其中活性成分為 65%; 氫氧化鎂母液,取自南陽雨豐化工生產車間,氯化銨質量濃度為 160 g/L。
實驗原理: 菱苦土中的 MgO 活性成分與氫氧化鎂母液中的氯化銨反應,生成氯化鎂和氨。氨通過吸收制得氨水,所得含鎂溶液可循環用于鎂化合物的制備。反應式如下:
MgO + 2NH4Cl →MgCl2+ 2NH3↑ + H2O
實驗方法: 量取氫氧化鎂母液 250 mL,按計算量加入菱苦土,加熱攪拌,反應結束后進行真空抽濾,獲得少量濾渣及二次殘液。二次殘液主要成分為 MgCl2,作為制備氫氧化鎂或堿式碳酸鎂的原料循環使用,分解過程排出的氨氣以水為吸收劑,經吸收器吸收制得氨水。氨水作為沉淀劑用于氫氧化鎂的制備。
1.2 分析方法
對含銨廢液和處理后溶液中氯化銨濃度的分析采用中和法。對菱苦土中氧化鎂含量及處理后溶液中鎂離子濃度的測定采用 EDTA 法。
2 結果與討論
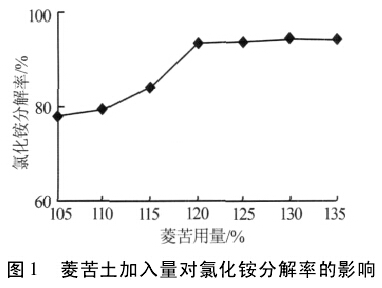
2.1 菱苦土加入量對氯化銨分解率的影響固定條件: 反應溫度為 85 ℃,反應時間為120 min。考察菱苦土用量對氯化銨分解率的影響,結果見圖 1。菱苦土用量( 以活性氧化鎂計) 為理論量的 105%、110%、115%、120%、125%、130% 和135% 。由圖 1 可以看出: 隨著菱苦土加入量的增加,氯化銨的分解率升高; 當菱苦土加入量為理論量的 120%時,氯化銨的分解率達到 93.7%; 之后再增加菱苦土的用量對分解率影響不大。因此確定菱苦土的最佳用量為理論量的 120%。
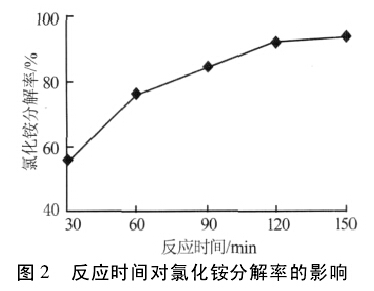
2.2 反應時間對氯化銨分解率的影響
固定條件: 菱苦土加入量為理論量的 120%,反應溫度為 85 ℃。考察反應時間對氯化銨分解率的影響,結果見圖 2。由圖 2 可以看出,隨著反應時間的延長分解率上升,當反應時間為 120 min 時氯化銨分解率達到91% 以上,繼續增加反應時間對氯化銨分解率影響不大。因此確定反應時間為反應溫度達到 85 ℃以后的 120 min。
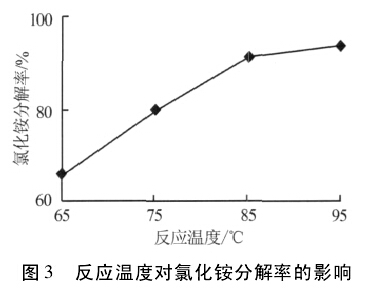
2.3 反應溫度對氯化銨分解率的影響
固定條件: 菱苦土加入量為理論量的 120%,反應時間為 120 min。考察反應溫度對氯化銨分解率的影響,結果見圖 3。由圖 3 看出,隨著反應溫度的升高氯化銨的分解率上升,當反應溫度為85 ℃時氯化銨分解率達到 90%以上,繼續升高反應溫度氯化銨分解率變化不大。因此確定反應溫度為 85 ℃。
3 結論
以菱苦土分解氫氧化鎂母液中氯化銨的最佳工藝條件: 菱苦土加入量( 以活性 MgO 計) 為理論量的 120%,反應時間為 120 min,反應溫度為 85 ℃。此條件下氯化銨的分解率達到 90% 以上。上述工藝條件的確定,為以氨法制備氫氧化鎂或以碳銨法制備堿式碳酸鎂生產過程中工藝廢水的處理奠定了理論基礎,也為氨的回收及循環利用提供了條件。此外,處理后所得溶液中含 Mg2+質量濃度在 38 g/L以上,可循環用于鎂化合物的制備。以菱苦土處理含銨廢水具有處理成本低、產物可循環利用、對環境無明顯污染等優勢。
參考文獻:
[1] 胡慶福,李寶林,李國庭,等. 醫用重質碳酸鎂制備的研究[J].無機鹽工業,1993( 1) : 20 -22.
[2] 胡慶福. 鎂化合物生產應用[M]. 北京: 化學工業出版社,2004: 340.



